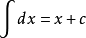阿伏加德罗常数的公式为:NA=N/n(NA:阿伏加德罗常数,N:粒子数,n:物质量)。 NA的近似值是6.02×10^23mol^-1。阿伏伽德罗常数因阿莫迪欧·阿伏伽德罗得名,他是一名19世纪早期的意大利化学家。
阿伏伽德罗常数公式
1.阿伏加德罗常数公式
阿伏加德罗常数的公式为:NA=N/n(NA:阿伏加德罗常数,N:粒子数,n:物质量)。 NA的近似值是6.02×10^23mol^-1。
2.阿伏伽德罗常数是多少?
阿伏加德罗常数,原名阿伏加德罗常数阿伏加德罗常数,是一个热常数,符号为NA。 其值一般计算为6.02×10²3或6.022×10²3。 它的正式定义是0.012kg碳12中所含的碳12原子数。
阿伏加德罗常数转换公式:n=N/NA=m/M=V/Vm=C*V
阿伏加德罗常数 0 所含的原子数称为阿伏加德罗常数。 阿伏加德罗常数的符号是NA。 阿伏加德罗常数的近似值为:6.02×10^23/mol。 符号:NA 含义:1 mol 任何粒子中所含的粒子数为阿伏伽德罗常数。
阿伏加德罗常数的定义值是指其中所含原子的数量。 值6.02×1023是阿伏加德罗常数的近似值。 两者之间是有区别的。 阿伏加德罗常数的符号是NA,它不是纯数,单位是mol-1。 阿伏加德罗常数可以通过多种实验方法测量。
阿伏伽德罗常数历史
阿伏伽德罗常数因阿莫迪欧·阿伏伽德罗得名,他是一名19世纪早期的意大利化学家,在1811年他率先提出,气体的体积(在某温度与压力下)与所含的分子或原子数量成正比,与该气体的性质无关 [9] 。法国物理学家让·佩兰于1909年提出,把常数命名为阿伏伽德罗常量来纪念他 [10] 。佩兰于1926年获颁诺贝尔物理学奖,他研究一大课题就是各种量度阿伏伽德罗常量的方法 [11] 。
阿伏伽德罗常量的值,最早由奥地利化学及物理学家约翰·约瑟夫·洛施米特(Johann Josef Loschmidt)于1865年所得,他透过计算某固定体积气体内所含的分子数,成功估计出空气中分子的平均直径 [12] 。前者的数值,即理想气体的数量密度,叫“洛施米特常数”,就是以他命名的,这个常数大约与阿伏伽德罗常量成正比。由于阿伏伽德罗常量有时会用 L 表示,所以不要与洛施米特(Loschmidt)的 L 混淆,而在德语文献中可能时会把它们都叫作“洛施米特常数”,只能用计量单位来分辨提及的到底是哪一个。
要准确地量度出阿伏伽德罗常量的值,需要在宏观和微观尺度下,用同一个单位,去量度同一个物理量。这样做在早年并不可行,直到1910年,罗伯特·密立根成功量度到一个电子的电荷,才能够借助单个电子的电荷来做到微观量度。一摩尔电子的电荷是一个常数,叫法拉第常数,在麦可·法拉第于1834年发表的电解研究中有提及过。把一摩尔电子的电荷,除以单个电子的电荷,可得阿伏伽德罗常量 [14] 。自1910年以来,新的计算能更准确地确定,法拉第常数及基本电荷的值(见下文#测量)。
让·佩兰最早提出阿伏伽德罗数( N )这样一个名字,来代表一克分子的氧(根据当时的定义,即32克整的氧) [10] ,而这个词至今仍被广泛使用,尤其是入门课本 [15] 改用阿伏伽德罗常量( N A )这个名字,是1971年摩尔成为国际单位制基本单位[16] 后的事,因为自此物质的量就被认定是一个独立的量纲[17] 。于是,阿伏伽德罗数再也不是纯数,因为带一个计量单位:摩尔的倒数(mol −1 )。