高中化学方程式非常多,一不小心就搞混了。因此小编整理了以下化学方程式记忆方法,供参考。
实验联想法
从生动直观到抽象思维,化学方程式是化学实验的忠实和本质的描述,是实验的概括和总结。因此,依据化学实验来记忆有关的化学反应方程式是最行之有效的。例如,在加热和使用催化剂(mno2)的条件下,利用kclo3分解来制取氧气。只要我们重视实验之情景,联想白色晶体与黑色粉末混和加热生成氧气这个实验事实,就会促进对这个化学反应方程式的理解和记忆:
反应规律法
化学反应不是无规律可循。化合、分解、置换和复分解等反应规律是大家比较熟悉的,这里再强调一下氧化——还原反应规律。如,fecl3是较强的氧化剂,cu是不算太弱的还原剂,根据氧化——还原反应总是首先发生在较强的氧化剂和较强的还原剂之间这一原则,因而两者能发生反应:
2fecl3+cu=cucl2+2fecl2
而相比之下,cucl2与fecl2是较弱的氧化剂与还原剂,因而它们之间不能反应。
根据物质的分类记忆
掌握此类方法的关键是要熟练掌握酸、碱、盐及氧化物这几个概念。同类物质一般都具有相似的性质,记住一个方程式也就记住了一类方程式。如co2能和naoh反应:co2+2naoh=na2co3+h2o,对这个方程式我们不能只把它看成一个方程式,要从分类法的角度去看它,其中co2属于酸性氧化物,naoh属于碱,这个方程式代表一类方程式即:酸性氧化物+碱=盐+水。如so2、so3都属于酸性氧化物,因此他们都可与碱反应生成相应的盐和水:so2+2naoh=na2so3+h2o,so3+2naoh=na2so4+h2o。
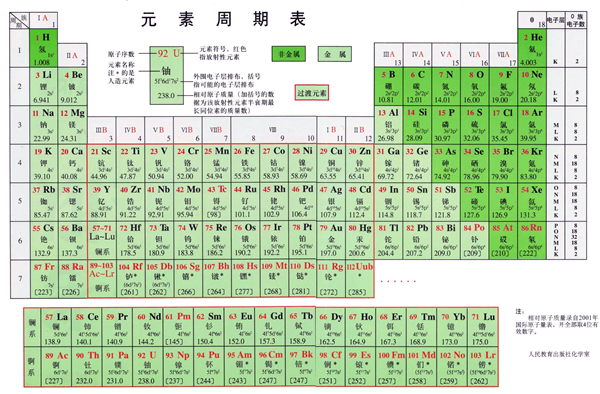
根据元素的位置记忆
如在周期表中处在同一列的主族元素,由于最外层电子数相同因此具有相似的性质。如第一列的碱金属元素都能和水反应生成相应的碱和氢气,卤族元素单质都能和氢气反应生成相应的氢化物等。
特例记忆法:特殊反应,特殊关照
有些特殊的、不符合一般规律的反应,往往成为高考的最爱,常考常新,所以这类反应就需要我们的特殊关照,特别记忆。记忆时对其多联系、多分析,知道它们的特殊所在,就有助于加深我们的记忆。
例如:铝与氢氧化钠溶液的反应,按照一般的规律金属是不能和碱溶液反应的,铝为什么能反应呢?为了更好的说明原因,其过程可分解为两步:
第一步:2al+6h2o=2al(oh)3+3h2↑,这一步符合活泼金属与水的反应规律。
第二步:al(oh)3+naoh=naalo2+2h2o,这一步符合氢氧化铝的两性,氢氧化铝溶解生成了易溶的偏铝酸钠,金属铝裸露出来就可以继续与水反应了。
两个方程式经过相加,消去两边相同的al(oh)3即可得到铝与氢氧化钠溶液的反应方程式:2al+2naoh+2h2o=2naalo2+3h2↑。
知道了这两步反应过程,学生就能更加深刻地理解铝与氢氧化钠溶液的反应,从而有助于加深记忆。再比如,过氧化钠与水的反应也是分两步进行的,道理一样,这儿不再赘述。
所以,对于这些特殊的化学反应,我们采取“特殊关照”的方法,对其多联系多分析,挖掘其“特殊”背后的东西,搞清其“特殊”背后的“不特殊”,我们的记忆就会变得更加深刻。
小编推荐:
“特征反应”记忆法:抓住官能团,记忆不再难
对于有机化学反应方程式宜采用特征反应记忆法。有机化学基本反应类型包括:取代反应、加成反应、加聚反应、消去反应、酯化反应、缩聚反应等。
每一类有机物都可发生其对应的特征反应,抓住这些特征反应,就有利于记忆有机化学反应方程式。
比如烷烃可发生取代反应;烯烃可发生加成反应、加聚反应;卤代烃、醇可发生消去反应;醇、羧酸可发生酯化反应等等。
这些特征反应实际上是由有机物中的官能团决定的,抓住了官能团就抓住了特征反应,也就容易记忆方程式了。
反复记忆法
有句话叫做:一回生,二回熟,三回见面是“仁兄”,这句话放在记忆方程式上也有道理,“多次见面,混个脸熟”对记忆化学方程式不失为一个好方法。多次见面并且重复的记忆有助于把暂时记忆转化为永久性记忆。